جوش شیرین (بیکربنات سدیم ) چیست؟

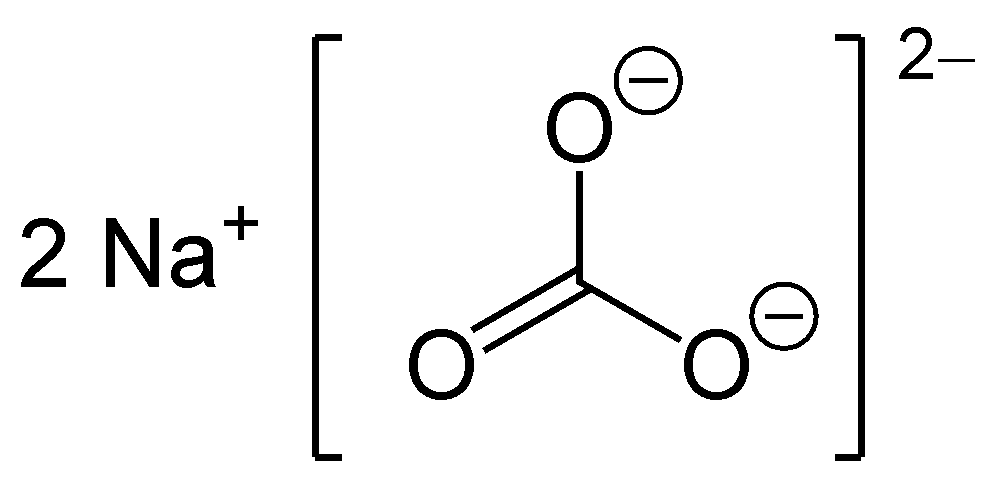
بیکربنات سدیم ( NaHCO3 )، نمک یک سدیمی اسیدکربنیک میباشد.
این ترکیب ، در بین عموم مردم به جوش شیرین معروف است
و معمولا در ترکیب خمیر نان ، برای متخلخل کردن نان استفاده میشود.
معمولا به صورت پودر سفید یا به صورت کریستالی یافت میشود.
این ترکیب بدون بو و طعم میباشد و دارای قلیائیت ناچیزی است
و به عنوان یک آنتی اسید ،
برای کم کردن اسید معده و درمان سوزش آن بکار میرود.
بیکربنات سدیم ، جاذب رطوبت و بوگیر خوبی میباشد
و از جعبههای حاوی این ترکیب میتوان
در یخچال ، برای جذب بو استفاده کرد.
بیکربنات سدیم بطور طبیعی در چشمههای آب معدنی یافت میشود
و به صورت مصنوعی هم سنتز میشود.
با عبور دادن گاز CO2 از داخل محلول جوشان
کربنات سدیم خالص یا محلول هیدروکسید سدیم ،
بیکربنات سدیمبه صورت رسوب تهنشین میشود.
بیکربنات سدیم همچنین به عنوان فراورده فرعی
درفرآیند سالوی تهیه میشود. در این فرآیند ،
کلرید سدیم باآمونیاک و کربن دی اکسید وارد واکنش میشود
و بیکربنات سدیم به صورت رسوب تهنشین میشود
که رسوب را بعد از صاف کردن و خشک کردن
در اثر حرارت به کربنات سدیم تبدیل میکنند.
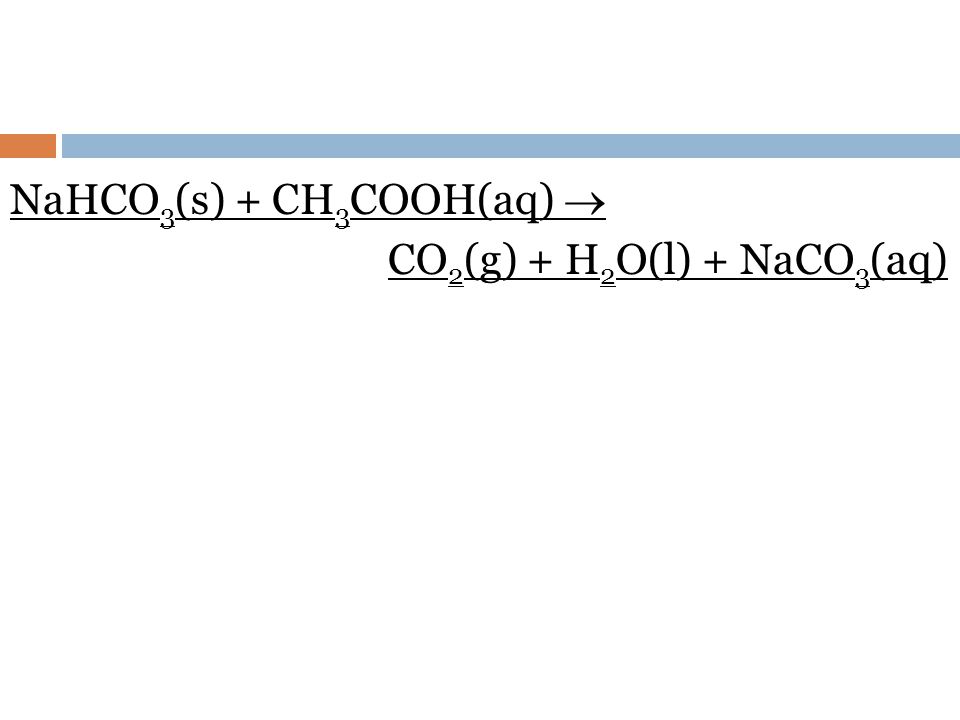
به سادگی جوش شیرین یا سدیم بیکربنات را در یک کوره
در دمای 200درجه فارنهایت( 93 درجه سلسیوس)
در حدود یک ساعت حرارت دهید.
کربن دی اکسید و آب بیرون خواهند رفت
و سدیم کربنات خشک باقی خواهد ماند.
بیشترین استفاده از بیکربنات سدیم ،
در تهیه انواع بکینگ پودر میباشد.
مقدار اضافی از خمیر جوش شیرین ،
بطور مؤثر در پاک کردن
و سائیدن سطوح میتواند مورد استفاده قرار گیرد.
استفاده از این ماده در ترکیب خمیر دندان
به رفع تدریجی لکههای دندان و سفید شدن آنها کمک میکند.
در صنایع غذایی ، تولید نوشابههای گازدار به عنوان
منبع CO2 ، صنایع پاک کنندههای خانگی
و در کپسولهای خاموش کننده آتش بکار میرود.
نخهای پشمی و ابریشمی استفاده میشود.
همچنین میتواند به عنوان پاک کننده و ساینده ملایم
در صورتیکه ایجاد حساسیت نکند برای زیبایی پوست بکار رود.
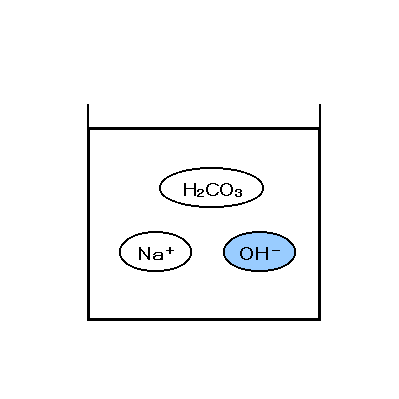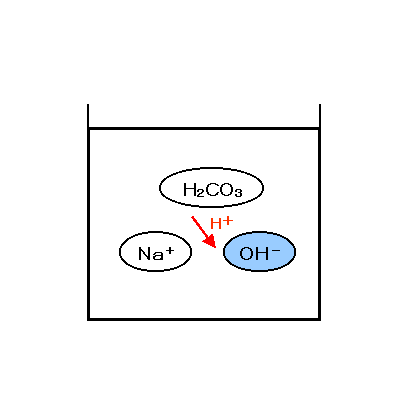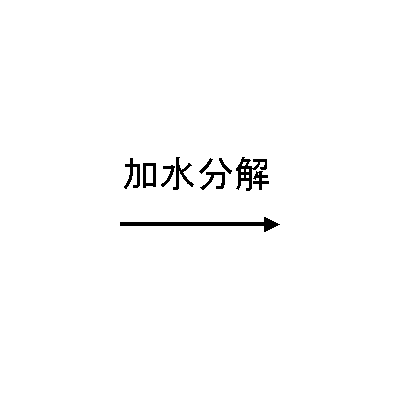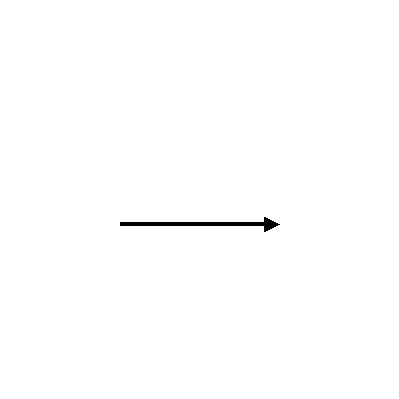
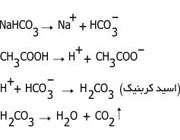
جوش شیرین در آب یک آمفوتر است.
یعنی در آب میتواند به عنوان اسید یا باز رفتار کند.
رفتار اسیدی آن به سبب وجود هیدروژن در ترکیبش است که در
صنایع مختلف به عنوان آزادکننده کاربرد دارد.








برای نمایش آواتار خود در این وبلاگ در سایت Gravatar.com ثبت نام کنید. (راهنما)






















































ایمیل شما بعد از ثبت نمایش داده نخواهد شد