اسید و آب ...
نظریه آرنیوس درباره اسیدها:
مطابق تعریف آرنیوس ،
اسید ماده ایست که در آب یونیزه میشود
و یون +H۳O که گاهی بصورت +H نیز نشان داده میشود، تولید میکند.
(HCl —–> H+ + Cl-(aq
آرنیوس قدرت اسیدی را نیز بر همین اساس تفسیر کردو گفت که
اسید قوی ، در محلولهای آبی تقریبا، بطور کامل یونیزه میشود.
در صورتیکه که میزان تفکیک اسید ضعیف کمتر است.
توجه کنید که مفهوم آرنیوس بر یونهای آب استوار است.
بر اساس تعریف آرنیوس میتوان نقش اکسیدهای اسیدی را نیز تفسیر کرد.
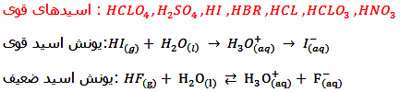
بازها و آب ...
باز در شیمی،
رایجترین برداشت از مادهای محلول است که
میتواند پروتونهارا بپذیرد.
از باز بیشتر بهعنوان یک قلیا نام میبرند
(تنها اگریونهایOH− در آن باشد).
این موضوع به
نظریه برونستد-لوری در مورداسیدها و بازها اشاره دارد.
در تعریف دیگر،
باز به هرترکیب شیمیایی گفته میشود که
وقتی در آب حل شد، به آن pH بیشتر از ۷٫۰ بدهد.
سدیم هیدرواکسید معروف به سود سوزآور وآمونیاک
نمونههایی از بازهای ساده هستند.
باز نقطهٔ مقابل اسید است؛
چون اسیدها غلظت یون هیدرونیم (H3O+) را در آب میافزایند
و بازها از غلظت این ماده میکاهند.
واکنش بین یک باز و یک اسید را خنثی سازی میگویند.
بازها با اسیدها واکنش میدهند تا
آب و نمک (یا محلولهای آنها) را تولید کنند.
حل شدن بازها در آب به صورت یک واکنش شیمیایی نبوده
و انحلال آنها فیزیکی است.
یعنی تنها تفکیک یونی صورت گرفته
و کاتیون فلز به همراه یون هیدروکسید (OH-)
به صورت محلول آزاد میشوند.
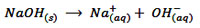
یک باز ممکن است در آب محلول یا نامحلول باشد.
به بازهای محلول در آب قلیا می گویند.
مهمترین قلیاها،
هیدروکسیدهای گروههای 1 و 2 جدول تناوبی
(به جز Be و Mg) هستند.
مثال:
Fe(oH)3 با اینکه یک باز است
امّا قلیا محسوب نمیشود،
زیرا در آب نامحلول است.