مروری بر خاصیت کشش سطحی آب


کشش سطحی ( Surface tension)
آیا میدانید
چرا وقتی سوزن خشکی را به آرامی بدون اینکه دستمان با آب برخورد کند
روی آب قرار دهیم، بدون اینکه به ته آب سقوط کند روی آن شناور باقی میماند؟
این امر نشانگر چیست ؟
چرا برخی حشرات به راحتی میتوانند روی سطح آب بایستند؟
بسیار دیده ایم که بامدادان قطره های درشتی از ژاله
یا شبنم روی برگ یا گلبرگ گیاهان شکل گرفته اند ,
معمولا چون این قطره ها کم کم شکل میگیرند
به دانه های نسبتا برزگی بدون اینکه فرو بریزند تبدیل میشوند
و بصورت کرهء (ضم کاف) پهن شده ای در میایند .
روی برگ های گل لادن همیشه دیده ام که آنها درشت تر هستند ,
این بخاطر فشار ملوکولی آبست که جاذبه ای ایجاد میکند
که مولوکولها را به طرف داخل کره میکشد
و آنرا به حالت کروی در میاورد
اگر شما با یک قطره چکان قطره کوچکی الکل روی آن بریزید
بواسطهء کوچک بودن مولکولهای الکل و نفوذ آن در آب
این فشار به هم خورده و باعث ریزش شبنم میشود
اگر در یک روز تابستانی به سطح آب برکهای نگاه کنید
احتمالاً حشره های زیادی را می بینید که
روی سطح آب راه میروند درست همان طور که شما میتواند
روی یک تخت فلزی بزرگ راه بروید.
تیغ ریشتراشی یا یک سوزن خیاطی را،
اگر چه چگالی فولاد تقریباً پنج برابر بیشتر از چگالی آب است،
میتوانید روی ظرف پر از آب شناور کنید.
قطرات آبی که از یک شیر آب، به آهستگی چکه میکند در نظر بگیرید،
هر قطره ابتدا به شکل تقریباً نیم کرهای درمیآید
و سپس هنگام جدا شدن از شیر به شکل کره در میآید.
اینها و بسیاری از پدیده های دیگر ناشی از کشش سطحیاند.
اما علت کشش سطحی چیست؟
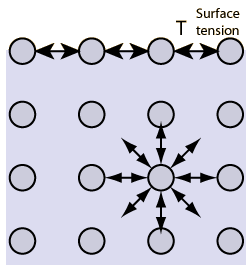
کشش سطحی ( Surface tension)
ویژگیای در مایعها است که باعث میشود
لایه بیرونی آنها به صورت ورقهای کشسان عمل کند.
این همان ویژگیای است که موجب ربایش دو سطح مایع به یکدیگر میشود؛
مانند دو قطرهٔ آب که همدیگر را میربایند و قطرهٔ بزرگتری میسازند.
هر مولکول مایع از سوی مولکولهای دیگرِ مایع ربوده میشود.
مولکولهایی که درون حجم مایع هستند، از همه جهت ربوده میشوند
و برایند نیروی وارد به آنها صفر است.
اما مولکولهایی که در سطح مایع هستند
تنها از یک جهت از سوی دیگر مولکولها ربوده میشوند
و نیروی ربایش در آن سوی مرز مایع
مثلاً از طرف مولکولهای هوا به آنها کمتر است.
بنابراین، به مولکولهای روی سطح مایع
نیروی خالصی به سمت درون وارد میشود
که این نیرو با مقاومت مایع در برابر فشردهشدن خنثی میشود.
در نتیجه، نیرویی در مایع به وجود میآید که میخواهد سطح مایع را کم کند.
از همین رو سطح مایع به شکل ورقهای الاستیک عمل میکند
و آن قدر جمع میشود که کمترین سطح ممکن را داشته باشد.
راه دیگر برای توضیح کشش سطحی این است که
یک مولکول اگر در کنار مولکول همسایهاش باشد،
انرژیاش کمتر از وقتی است که کنار آن همسایه نباشد.
مولکولهای درونی بیشترین تعداد همسایههای ممکن را دارند.
ولی مولکولهایی که در سطح هستند همسایههای کمتری دارند
و بنابراین انرژیشان بیشتر از انرژی مولکولهای درونی است.
بنابراین، وقتی که مایع میخواهد انرژی کلاش را کمینه کند،
میکوشد تا از شمار مولکولهای سطحیاش بکاهد،
و این یعنی یک مایع میخواهد کمترین سطح ممکن را داشته باشد.
برای کاستن از سطح، یک مایع
همیشه هموارترین شکل ممکن را در سطح خود میگیرد.
هر خمیدگی تازه بر روی سطح به مساحت بیشتر
و در نتیجه انرژی بیشتر میانجامد.
اگر بخواهیم رویهٔ دوبعدیای را بیابیم که
میان مرزهای مشخصی قرار بگیرد
و کمترین سطح ممکن را داشته باشد،
شاید با ریاضیات به سختی به نتیجه برسیم.
ولی به جایش میتوانیم مرزها را با سیم بسازیم
و آن را درون ظرفی پر از آب و صابون فرو ببریم.
لایهٔ حباب صابونی که بین سیمها ساخته میشود
به تقریب نشاندهندهٔ رویهای با کمترین سطح ممکن است
اگر گرانش زمین نبود دقیقاً کمترین سطح را میساخت.
بنابراین بطور خلاصه میتوان گفت :
وقتی گازی را فشرده و سرد میکنیم
با نزدیک شدن مولکولها به هم
نیروی ربایشی بین آنها افزایش پیدا میکند
و در دما و فشار خاصی گاز به مایع تبدیل میشود.
هر مولکول در داخل مایع از همه طرف
توسط مولکولهای دیگر محصور شدهاست
و از همه طرف، نیروی ربایشی
از طرف سایر مولکولهای دیگر بر آن وارد میآید.
به علت تقارن برآیند این نیروها صفر است،
یعنی هر نیرو با نیروی مساوی و هم اندازه
ولی در جهت مخالف خنثی میشود.
ولی برای یک مولکول که در سطح مایع قرار دارد این تقارن وجود ندارد
زیرا از اثر مولکولهای هوا که ناچیزند چشم پوشی شده است
و هر مولکول از طرف نصف تعداد مولکولهای
مجاور یک مولکول واقع در داخل مایع، نیروی ربایشی وارد میشود.
برآیند این نیروها، نیروی عمود بر سطح به سمت داخل مایع است.
این نیرو را، نیروی کشش سطحی گویند.
در غیاب نیروهای خارجی این نیرو
عامل شکل کروی هر جرمی از مایع است
تا نسبت حجم به سطح حداکثر شود
و سطح آزاد مایعها دارای کمترین مساحت ممکن باشد.
در این حالت سطح مایع مانند یک پوستهی کشیده رفتار میکند.
نظر به اینکه در اجسام هم حجم که دارای اشکال گوناگون هستند
کره کمترین سطح کشیده را دارد،
مایعها به صورت قطرههای کروی در میآیند.
برای نمایش آواتار خود در این وبلاگ در سایت Gravatar.com ثبت نام کنید. (راهنما)




















































ایمیل شما بعد از ثبت نمایش داده نخواهد شد