جدول تناوبی عناصر، آرایشی ازعنصرهای شیمیایی به صورت تناوبها یادورهها ( ردیفها )،و گروهها (ستونها ).مندلیف پیشنهاد کرد که عنصرها باید به ترتیبافزایش جرم (وزن) اتمی منظم شدهو بر طبق خواصشان گروهبندی شوند.این جدول بر اساس قانون تناوبی عنصرها استوار است.بر طبق این قانون هرگاه عنصرها رابر حسب افزایش عدد اتمی در کنار یکدیگر قرار دهیمخواص فیزیکی و شیمیایی آنها به صورت تناوبی تکرار میشود.
در مرکز اتم یک هسته وجود دارد.بیشتر جرم و تمام بار مثبت اتم در این هسته متمرکز است.امروز اعتقاد بر این است کههسته از تعدادی پروتون و نوترون تشکیل میشودکه مجموعاً جرم آن را به وجود میآورند.پروتونها علت وجود بار مثبت در هسته میباشند.
الکترونها که بیشتر حجم اتم را اشغال میکنند.در خارج هسته (برون هستهای) میباشندو با سرعت به دور آن میگردند.از آنجا که هر اتم از نظر بار الکتریکی خنثی است،کل بار مثبت هسته که از پروتونهای آن ناشی میشود،معادل کل بار منفی تمام الکترونهاست،بنابراین تعداد الکترونها برابر تعداد پروتونهاست
پیوندها
- علوم و روش آموزش آن به کودکان و نوجوانان
- طراحی و تصویر سازی
- olume parsa book
- اسلاید های آموزشی علوم شما می توانید مستقیما تمام اسلاید های آموزشی علوم و در زمینه هنری را در این سایت در بخش فارسی زبانان مشاهده کنید
- آموزشی و علمی آموزش علوم
- amoozesholume.blogspot.com آموزش علوم
جدیدترین یادداشتها
همه- History of the atom 5
- History of the atom 5
- اسلاید آموزشی(Google slides)-تاریخچه اتم-5
- اسلاید آموزشی(انیمیشن )-تاریخچه اتم -5
- تاریخچه اتم -5
- Speed of light -۴
- HISTORY OF THE ATOM- (4)
- History of the atom 4
- اسلاید آموزشی(Google slides)-تاریخچه اتم-4
- تاریخچه اتم -4
- اسلاید آموزشی(انیمیشن )-تاریخچه اتم -4
- History of the atom 3
- اسلاید آموزشی(Google slides)-تاریخچه اتم-3
- HISTORY OF THE ATOM- (3)
- تاریخچه اتم -3
بایگانی
- اسفند 1400 5
- دی 1400 23
- آذر 1400 18
- آبان 1400 9
- مهر 1400 3
- شهریور 1400 6
- مرداد 1400 7
- خرداد 1400 18
- اردیبهشت 1400 18
- فروردین 1400 32
- اسفند 1399 51
- بهمن 1399 37
- دی 1399 38
- آذر 1399 37
- آبان 1399 31
- مهر 1399 32
- شهریور 1399 30
- مرداد 1399 30
- تیر 1399 53
- خرداد 1399 78
- اردیبهشت 1399 123
- فروردین 1399 115
- اسفند 1398 118
- بهمن 1398 116
- دی 1398 77
- آذر 1398 60
- آبان 1398 71
- مهر 1398 67
- شهریور 1398 86
- مرداد 1398 67
- تیر 1398 87
- خرداد 1398 91
- اردیبهشت 1398 99
- فروردین 1398 90
- اسفند 1397 89
- بهمن 1397 108
- دی 1397 93
- آذر 1397 83
- آبان 1397 65
- مهر 1397 63
- شهریور 1397 54
- مرداد 1397 85
- تیر 1397 75
- خرداد 1397 87
- اردیبهشت 1397 62
- فروردین 1397 76
- اسفند 1396 53
- بهمن 1396 72
- دی 1396 93
- آذر 1396 62
- آبان 1396 64
- مهر 1396 68
- شهریور 1396 55
- مرداد 1396 42
- تیر 1396 45
- خرداد 1396 49
- اردیبهشت 1396 45
- فروردین 1396 41
- اسفند 1395 28
- بهمن 1395 28
- دی 1395 30
- آذر 1395 53
- آبان 1395 49
- مهر 1395 44
- شهریور 1395 44
- مرداد 1395 58
- تیر 1395 58
- خرداد 1395 47
- اردیبهشت 1395 46
- فروردین 1395 47
- اسفند 1394 36
- بهمن 1394 40
- دی 1394 38
- آذر 1394 43
- آبان 1394 33
- مهر 1394 37
- شهریور 1394 37
- مرداد 1394 46
- تیر 1394 33
- خرداد 1394 39
- اردیبهشت 1394 35
- فروردین 1394 30
- اسفند 1393 32
- بهمن 1393 32
- دی 1393 29
- آذر 1393 35
- آبان 1393 41
- شهریور 1393 10
- مرداد 1393 5
- فروردین 1393 11
- اسفند 1392 10
- بهمن 1392 16
- دی 1392 15
- آذر 1392 16
- آبان 1392 12
- مهر 1392 10
- شهریور 1392 15
- مرداد 1392 23
- تیر 1392 22
- خرداد 1392 72
- اردیبهشت 1392 10
- فروردین 1392 15
- اسفند 1391 23
- بهمن 1391 57
- دی 1391 107
- آذر 1391 41
- فروردین 1390 4
شمارش پروتون، نوترون و الکترون
الکترون:
یک ذره درون اتمی است که
حامل بار الکتریکی منفی میباشد.
این ذره توسط گروهی از فیزیکدانان انگلیسی،
که تامسون نیز جزء آنان بود، در سال 1897 کشف شد.
پروتون:
ذراتی با بار مثبت که دقیقاً یک یون مثبت هیدروژن هستند.
ارنست رادرفورد در سال 1918 وجود این ذرات را گزارش داد.
او با فرستادن ذرات آلفا در گاز نیتروژن این مسأله را اثبات کرد.
نوترون:
ذرات درون اتمی بدون بار هستند که
در مرکز هسته اتمها قرار گرفتهاند.
این ذرات توسط جیمز چادویک در سال 1932 کشف شدند.
تعداد پروتونها = عدد اتمی
تعداد الکترونها = تعداد پروتونها = عدد اتمی
تعداد نوترونها = عدد جرمی – عدد اتمی
عدد جرمی = مجموع تعداد پروتونها و نوترونها
مثال:
عدد اتمی (Z)
به تعداد پروتون های هر اتم(به تعداد بارهای مثبت اتم) عدد اتمی می گویند
برای مثال اتم سدیم 11 پروتون دارد, پس عدد اتمی سدیم 11 است.
عدد اتمی را گوشه پایین سمت چپ نماد شیمیایی می نویسند 11Na
عدد جرمی (A)
به مجموع تعداد پروتون ها و نوترون های یک اتم عدد جرمی گفته می شود.
تمام اتم های یک عنصر پروتون های یکسان دارند اما تعداد نوترون های آن ها می تواند متفاوت باشد.
عدد جرمی در گوشه بالا و سمت چپ نماد شیمیایی نوشته می شود
مثلا اتم کربن در هسته خود 6 پروتون و 6 نوترون دارد
پس عدد جرمی آن 12 است. 12C
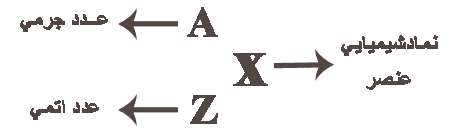
برای پیدا کردن تعداد پروتونها، الکترونها و نوترونهای یونها،
لازم است که:
کاتیونها (یونهای مثبت)
و آنیونها (یونهای منفی) را بشناسیم.
کاتیونها:
یونهایی که بار مثبت دارند کاتیون نامیده میشوند.
وقتی الکترونهای اتم از دست میرود کاتیون بوجود میآید.
آنیونها:
یونهای با بار منفی هستند که
درنتیجه وارد شدن الکترون اضافی به اتم تشکیل میشوند.
یون Na+ را درنظر بگیرید.
میدانیم که عدد اتمی
هر ساختار اتمی عنصر سدیم 11 است.
علیرغم این، به دلیل که اینکه
یون سدیم حامل بار مثبت میباشد،
باید یک پروتون اضافی داشته باشد
و یا اینکه یک الکترون از دست داده باشد.
از آنجاییکه سدیم نمیتواند پروتون بدست آورده باشد،
وگرنه تبدیل به منیزیوم میشود،
باید یک الکترون از دست داده باشد.
بنابراین:
تعداد پروتون و الکترونهای سدیم در اصل همان 11 است.
منتها چون یک الکترون از دست داده،
تعداد الکترونها = تعداد پروتونها = عدد اتمی = 10.
به همین ترتیب تعداد نوترون در یون سدیم برابر است با:
عدد جرمی – عدد اتمی = 10 – 23 = 13.
با بکار بردن جدول تناوبی عناصر، تشخیص
تعداد الکترون و پروتون و نوترون عناصر بسیار ساده میشود.
در این جدول عدد جرمی و عدد اتمی عناصر نوشته شده است.
اگر سعی کنید تعداد این ذرات درون اتمی را برای
چند عنصر دیگر نیز محاسبه کنید
در این روش ساده کاملاً حرفهای خواهید شد.
مرسی
عالی بود توی چند سایت رفتم ولی زیاد نفهمیدم این یکی عالی بود :
عالی بود عالی عالی :خوشتیپ
:خوشتیپ


عالی بود!!
عالی بود
عااااااالی
عالی بود





























میشه بگین ی یونی ک عدد اتمیشو نداریم فقط عدد جرمیشو داریم چطور حساب کنیم؟سوال اینه:یونM+۳با عددجرمی ۴۷،تعداد نوترون آن ۲۰ درصد بیشتر از تعداد پروتون ها باشد عدد اتمی این عنصر چقدر است؟
لطفا راهنماییم کنید☹
از این فرمول کمک بگیر مثل معادله ریاضی حل کنید.
تعداد پروتونها (p)-– (47)عدد جرمی = (p20%)تعداد نوترون
با نام خدا
به نظرم همه اموزشهایتان مختصر و مفید است و بدرد میخورد. با تشکرد
میشه یه فرمول خیلی راحت تر بگین
میشه بگین که که تعداد پروتون ها و نوترون و الکترون های 39k19 چند تاست
فلز قلیلیی گروه اول جدول تناوبی
ظرفیت یک چون در لایه ظرفیتی یک الکترون دارد
عدد اتمی ۱۹
عدد جرمی ۳۹
عدداتمی = تعداد پروتون= تعداد الکترون در حالت خنثی و اتم =۱۹
برای پیدا کردن تعداد نوترون کافی است عدد اتمی منهای عدد جرمی کنید.
۳۹-۱۹=۲۰
عدد اتمی: ۱۹
عدد جرمی استاندارد: ۳۹٫۰۹۸۳ g·mol−۱